APUNTS D'ESTEREOQUÍMICA
Dr. Eduard Bardají - Professor Titular de Química Orgànica - UdG
CONCEPTE D'ESTRUCTURA ORGÀNICA:
L'estructura dels compostos orgànics ve definida per la seva constitució que es concreta en una determinada proporció d'atoms (C, H, O, N, etc..) i es representa amb la seva formula molecular. El tipus d'enllaços entre atoms (sp3, sp2, sp) i la sequència amb que estan conectats entre ells, conectivitat i configuració, determinen l'estereoquímica de cada compost. En sentit ampli l'estructura d'un compost orgànic es defineix determinant la seva constitució i la seva estereoquímica.
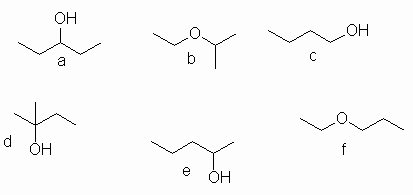
Els compostos a-f representats a continuació tenen la mateixa constitució. Tots tenen la mateixa formula molecular C5H12O, pero difereixen en la seva estereoquímica, o sigui pel tipus de conectivitat a la molecula. Per tant, a, b ,c , d, e , f són entre ells isòmers constitucionals (tambè isomers estructurals). Cadascun d'ells representa una única estructura possible excepte pel cas de e.

El compost e pot presentar, en el seu carboni substituit amb la funció OH, dues configuracions diferents: per tant la figura e representa dues estructures e1 i e2 que corresponen a compostos diferents.
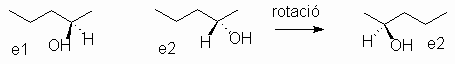
Si es compara e1 i e2 es veu que són diferents en la distribució dels substituents sobre el carboni 2. Quan s'intenta comparar les estructures e1 i e2 per sobreposició d'una sobre l'altre coincideixen dos substiuents pero els altres dos no coincideixen en cap cas; e1 i e2 són, en sentit ampli, estereoisomers o isòmers configuracionals, i són estructures constitucionalment idèntiques que difereixen en la seva estereoquímica i per tant en la seva configuració (en aquest cas la diferència es de configuració d'un atom Csp3).
ISOMERIA
Els COMPOSTOS DIFERENTS que coincideixen en la FORMULA MOLECULAR poden tenir CONECTIVITAT IDENTICA o DIFERENT.
SI LA CONECTIVITAT ES DIFERENT seran isòmers
CONSTITUCIONALS o ESTRUCTURALS : com exemple compara les estructures
de ETANOL I DIMETILÈTER (click: fitxer ).
SI LA CONECTIVITAT COINCIDEIX ES PLATEGEN DOS
SITUACIONS:
IDENTICA CONECTIVITAT + IDENTICA CONFIGURACIÓ + DIFERENT CONFORMACIÓ: es tractarà del mateix compost, però formalment de dues conformacions diferentes, parlem d'isomers CONFORMACIONALS.
IDENTICA CONECTIVITAT +DIFERENT CONFIGURACIÓ: els compostos seran ESTEREOISOMERS O ISOMERS CONFIGURACIONALS.
ESTEREOISOMERIA
Els diferents ESTEREOISOMERS o ISOMERS CONFIGURACIONALS venen definits pel fet de que la molècula conté un numero determinat de CENTRES o ELEMENTS ESTEREOGÈNICS (n), en funció d'aquest número, el nombre màxim d'estereoisomers possibvle per a una estructura orgànica és 2n estereoisómers.
Inicialment asociarem els elements d'estereoisomeria a :
Centres estereogènics o estereocentres (que són els Csp3 amb quatre substituents diferents (*) , i la seva configuració pot ser etiquetada amb els descriptors R/S
La presencia de enllaços dobles C=C amb almenys un substituent diferent a cada costat també genera estereoisomeria, i en aquest cas la configuració del doble enllaç pot ser etiquetada amb els descriptors Z/E . (veure descriptors configuracionals: click fitxer )
Dit d'un altre manera, , els Csp3 substituits amb diferents substituents i els sistemes C=C amb almenys un substituent
diferent a cada costat són elements estereogènics, i la seva configuració diferent (R o S; Z o E) genera l'existència de diferents estereoisómers del mateix compost.
La presència d'elements estereogènics en una molècula pot donar lloc a que la molècula sigui quiral en alguns
casos (no tots!!) i d'altra banda cal avisar de que poden haver-hi estructures quirals que ho siguin sense tenir cap Csp3 estereogènic
(atropoisomeria).
La relació estereoquímica entre els diferents estereoisomers es pot generalitzar de la forma seguent:
Si la molècula només conté 1 Csp3
* , els possibles estereoisomers es redueixen a 2,
Enantiòmers: exemples són 1-bromo-1-cloroetà,
Si la molècula conté 2 o més Csp3 * , alhora els diferents estereoisòmers (2n ) guarden relacions estereoquímiques diferents, alguns són entre ells enàntiomers i d'altres són diastereómers o diastereoisòmers.
2-cloro-1-propanol 3-bromo-butà-2-ol 2-butè
Ac.2,3-dihidroxi-butadioic Ac.2metilbutenoic
1-bromo-1-fenil-2-propè 1,2-dimetilciclohexà Ac2,5-heptadiendioc
2-metil-3-hidroxipropanal 2,3,4,5-tetrahidroxipentanal
QUIRALITAT
Els objectes quirals en general, i les molècules en particular, tenen la propietat de ser diferents de la seva imatge de reflexió en un plà imaginari. Vulgarment es diu que sòn no "sobreposables" amb la seva imatge "especular".
Les nostres mans sòn objectes quirals i representen imatges especulars l'una de l'altre.
Les estructures de la figura (e1 i e2) sòn diferents i posades davant d'un plà de simetria representen l'imatge especular l'una de l'altre:
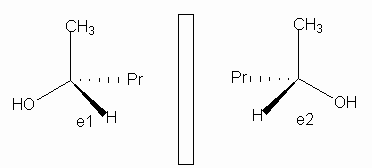
Cada compost ès un dels dos possibles estereoisòmers de1 2-butanol: (R)-2-butanol (e1) i (S)-2-butanol (e2). Tal com apareixen en la figura es veu la seva relació especular (enantio) i d'aquí ve el nom d'enantiomers per tots aquells compostos que sòn estereoisòmers i alhora sòn imatge especular l'un de l'altre.
Els enantiomers sòn estereoisòmers que tenen idèntiques propietats físiques i energètiques entre sí en general, i només sòn distingibles mitjançant medis quirals, com per exemple un polarimetre, cromatografia quiral o un enzim. Al polarimetre, els enantiomers mostren capacitat de girar el plà de la llum polaritzada i la seva activitat òptica rotatòria al polarimetre ès de la mateixa magnitud i de signe diferent per a cada enantiòmer ( en les mateixes condicions experimentals).
Els diastereòmers sòn estereoisòmers que tenen diferents propietats físiques i energètiques en general, i sòn distingibles mitjançant medis no quirals, com per exemple cromatografia convencional o reactius no quirals.
Ja hem comentat que el número total d'estereoisómers, enantiómers i diastereòmers, és de 2n (n= nº d'elements estereogènics). De tots els possibles estereoisomers d'un compost hi ha el cas especial de les formes meso: que sòn estructures amb un plà de simetria intern que, de fet, anula la existència de dos possibles estereoisòmers, en aquests casos el número total d'estereoisomers es menys de 2n, i també anula les propietats quirals de les molècules (no mostren activitat òptica al polarimetre).
La comparació de la relació estereoquímica entre diversos compostos és més fàcil quan es realitza comparant conformacions equivalents o be quan s'utilitzen projeccions equivalents de la seva estructura.
Quan l'anàlisi directe del model molecular tridimensional es complica, degut a que les estructures són complexes, la comparació de la relació estereoquímica entre diversos compostos es fa difícil, es adequat reduïr la complexitat estructural de les molecules a projeccions mes simples de manipular. Així les projeccions de cavallet, projeccions de Newman, projeccions de Fischer o projeccions de Haworth, ens permeten reduïr la complexitat estructural de la molecula a projeccions mes simples de manipular i ens faciliten l'anàlisi de les relacions d'estereoisomeria entre compostos.
Sempre que s'utilitzen projeccions cal tenir molt en compte els convenis que regeixen la formació de cada projecció i per tant la relació que hi ha entre l'estructura "real" i la "projectada".